文章插图
图1: 本文和前文报道的嘧啶核苷、嘌呤脱氧核苷的史前合成路线 。
这样以RAO为起始原料,与氰基乙炔(11)反应生成α-脱水胞苷 (12),再经过硫代(与硫化氢反应,硫化氢和二氧化硫可以由原始地球的火山活动得到)生成α-2-硫代胞嘧啶(13),可以通过光照把1′位构型反转得到β-2-硫代胞嘧啶(3) 。经过水解除了能得到嘧啶核糖核苷,胞嘧啶(1)和尿嘧啶(2)(也就是遗传密码中的C和U)外,还生成了2-硫代尿嘧啶(4) 。这种修饰的核苷在现代生物学的转运核糖核酸(t-RNA)中存在,在基因表达和指导蛋白质合成中扮演一定的作用 。在磷酸化的过程中,2-硫代尿嘧啶(4)发生分子内重排生成硫代脱水尿苷(6) 。而硫代脱水尿苷在光照下被硫化氢还原为2′-脱氧-2-硫代胞嘧啶(5),一个修饰的脱氧核苷 。5 再与腺嘌呤(8)发生碱基交换反应能低产率(4%)得到腺嘌呤脱氧核糖核苷(7, dA),但是同时得到更多的是它的端位异构体α-腺嘌呤脱氧核糖核苷(6%) 。这个光化学还原反应成功地将一个核糖核苷4经过硫代脱水核苷6,利用硫化氢作为还原剂,成功得到了相应的脱氧核糖核苷5 。总结于图2的这个过程提供了一个思路:脱氧核糖核苷可以由硫代脱水核苷经过硫化氢的光照还原反应得到 。
文章插图
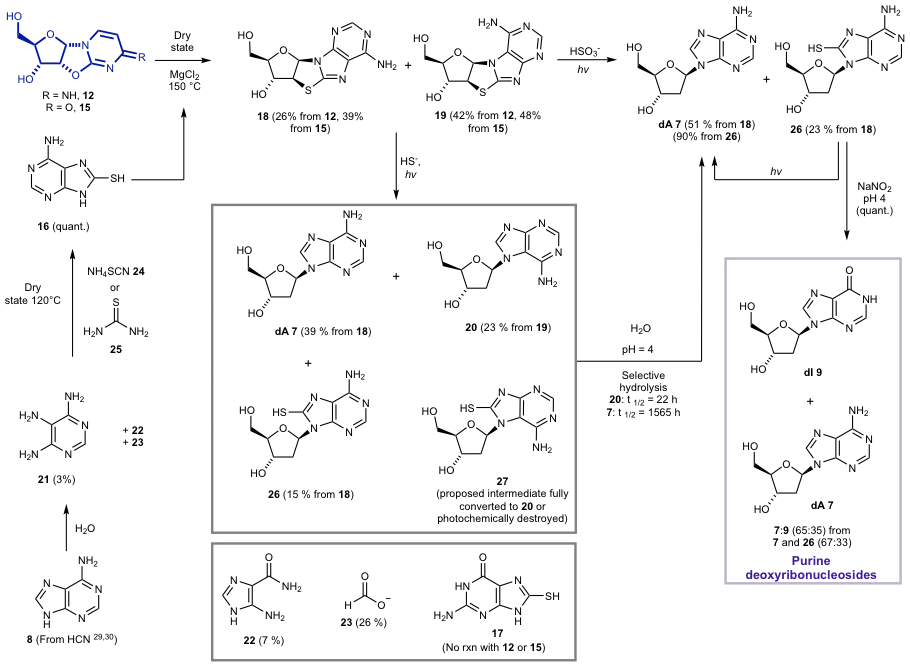
图2: 嘌呤脱氧核苷(dA, dI) 的史前合成路线 。
该文研究人员直接利用α-脱水胞苷 (12)或α-脱水尿苷 (15)作为糖基供体,8-巯基腺嘌呤为苷元,在干法加热中碱基交换分别以68% 和87% 的转化率得到硫代脱水嘌呤核苷 (18) 及其7位氮苷异构体 19 。虽然在碱基取代反应中,非天然的7位氮苷异构体19的产率要高于天然的9位氮苷18,但是在下一步与硫化氢的光化学还原反应中,18的转化率(39%)要远高于19的转化率(23%),分别生成天然的腺嘌呤脱氧核糖核苷(7, dA)和它的7位氮苷异构体20 。更值得注意的是,如果选择另一种还原剂亚硫酸氢根[8]进行光化学还原反应,这种化学选择性达到极致,非天然的7位氮苷异构体 19被完全降解,18 和19 的混合物只得到天然的9位氮苷产物7(dA) 。另外,在室温和弱酸性水溶液中,7的水解速率是其异构体20的1/70 。这些结果都说明,天然腺嘌呤核苷在人为条件和自然环境下均更为稳定 。在生命起源的历史长河中,自然界总能利用强大的化学选择性为生命体系挑选合适的分子结构,并保留在现代生物体中 。
在同样条件下以8-巯基鸟嘌呤(17)与12 或15反应并没有得到硫代脱水鸟嘌呤核苷,因此不能生成鸟嘌呤脱氧核苷(dG) 。但是脱氧腺苷7 可以在亚硝酸环境 (pH = 4) 脱氨水解,以40% 产率生成脱氧肌苷 (9, dI) 。近期有文献报道,肌苷(I)可以代替鸟苷(G)与胞嘧啶核苷高保真配对[9] 。相同的条件下,胞嘧啶(C)脱氨水解为尿嘧啶(U) 。这样作者成功实现了在同一体系中从α,β-2-巯基胞嘧啶核苷(13 和3的混合物)出发经过脱氨水解、高温共热、紫外光还原和再次脱氨水解四步高产率生成 dA、dI、C和U四种核苷的化学反应(图3) 。在这个过程中,立体选择性(β-或α-糖苷键)、区域选择性(腺嘌呤9- 或7- 取代)和呋喃环(五元环或六元环)选择性都得到了体现,在最终反应混合物中只有天然构型的核苷得以生成和保留 。混合产物中的嘧啶核糖核酸(C和U)和嘌呤脱氧核糖核酸(dA和dI)从理论上构成了另类的遗传信息字母表 。
文章插图
图3: 可能组成生命起源原始浓汤中遗传信息字母表的C, U, dA, dI 的系列合成 。
- 草和寇的成语 草什么为寇成语
- 中国有多少个省份和直辖市和自治区以及它们的简称 中国有多少个省份和直辖市
- 和谁开过房宾馆能查出来吗 可以查是和谁开的房吗
- 订桌和定桌 订与定的区别
- 5g的优势与弊端 5g和4g的区别
- 成考和网教的区别在哪 网教和成教的区别
- 计算机显卡的品牌 显卡n卡和a卡的区别
- 怎么区分485和232 232和485的区别
- 肉孜节和古尔邦节哪个是大年 肉孜节和古尔邦节哪个是大节
- 怎么查老公和别人的微信聊天记录 微信聊天记录怎么找回最早的记录