5、氢化铝锂(LiAlH4)是有机合成中的重要还原剂 。某课题组设计实验制备氢化铝锂并测定其纯度 。已知: 氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体 。
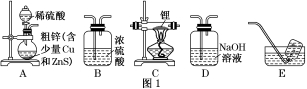
Ⅰ.制备氢化锂:选择图1中的装置制备氢化锂(有些装置可重复使用):
文章插图
文章插图
(1)装置的连接顺序(从左至右)为A→______________________________
(2)检查好装置的气密性 , 点燃酒精灯前需进行的实验操作是________________________________________
(3)写出制备氢化锂的化学方程式:_____________________________________________________
Ⅱ.制备氢化铝锂:1947年 , Schlesinger、Bond和Finholt首次制得氢化铝锂 , 其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合 , 搅拌 , 充分反应后 , 经一系列操作得到LiAlH4晶体 。
(4)写出氢化锂与无水三氯化铝反应的化学方程式:_______________________________________________
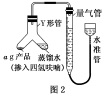
Ⅲ.测定氢化铝锂产品(不含氢化锂)的纯度
(5)按图2装配仪器、检查装置气密性并装好试剂(Y形管中的蒸馏水足量 , 为了避免氢化铝锂遇水发生爆炸 , 蒸馏水中需掺入四氢呋喃作稀释剂) , 启动反应的操作是______________________________________________ 。读数之前 , 上下移动量气管右侧的容器 , 使量气管左、右两侧的液面在同一水平面上 , 其目的是__________
________________________________
(6)在标准状况下 , 反应前量气管读数为V1 mL , 反应完毕并冷却之后 , 量气管读数为V2 mL 。该样品的纯度为______(用含a、V1、V2 的代数式表示) 。如果起始读数时俯视刻度线 , 测得的结果将________(填“偏高”“偏低”或“无影响”)
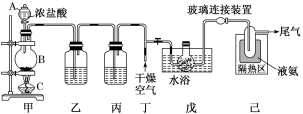
6、一氧化二氯(Cl2O)是一种氯化剂和氧化剂 , 极易溶于水 , 与水反应生成HClO , 遇有机物易燃烧或爆炸 。利用如图装置可制备Cl2O 。回答下列问题:
文章插图
已知Cl2O的部分性质如表:
熔点
沸点
制备方法
-120.6 ℃
2.0 ℃
2HgO+2Cl2===Cl2O+HgCl2·HgO
(1)装置甲中仪器B的名称是____________
(2)装置甲的作用是为该制备反应提供Cl2 , 写出该装置中制备Cl2的离子方程式:__________________________
(3)装置乙的作用是____________________ , 装置丙的洗气瓶中盛有的试剂是____________
(4)装置戊中的特型烧瓶内盛有玻璃丝 , 玻璃丝上附着有HgO粉末 , 其中玻璃丝的作用是___________________
(5)装置戊和装置己之间的装置为玻璃连接装置 , 而不是橡胶管 , 其原因是_________________________________
(6)氨的沸点为-33.4 ℃ , 熔点为-77.7 ℃ , 则装置己中收集到的产物为________(填“固体”“液体”或“气体”)物质 。
若实验开始前称量装置戊中的玻璃丝与HgO的混合物的质量为a g , 实验结束后玻璃丝及其附着物的质量为b g , 则制备的Cl2O为________mol
(7)尾气中的有毒气体成分是________ , 可用________吸收除去
7、实验室以绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe] 有关物质性质如下:
甘氨酸(NH2CH2COOH)
柠檬酸
甘氨酸亚铁
易溶于水 , 微溶于乙醇 , 两性化合物
易溶于水和乙醇 , 有强酸性和还原性
- 染发剂什么牌子好 染发剂排名第一
- 现在什么专业比较吃香 未来什么技术最吃香
- 春天开的常见的花的名字 春天开花的植物有哪些
- 什么叫绩效工资 员工绩效工资分配方案
- 送妈妈生日礼物送什么好 送妈妈礼物排行大全
- 三本和大专有什么区别 500分的大专和200分的大专
- 网络营销的方式包括哪些 简述网络营销的方式有哪些
- 4款实用的微信营销工具软件 微信推广软件有哪些
- 水果店进货渠道有哪些 水果批发商利润有多大
- 自然堂属于什么档次的护肤品 国产十大最有效抗衰老护肤品