易溶于水 , 难溶于乙醇
实验过程:
Ⅰ.配制含0.10 mol FeSO4的绿矾溶液
Ⅱ.制备FeCO3:向配制好的绿矾溶液中 , 缓慢加入200 mL 1.1 mol·L-1 NH4HCO3溶液 , 边加边搅拌 , 反应结束后过滤并洗涤沉淀
Ⅲ.制备(NH2CH2COO)2Fe:实验装置如下图(夹持和加热仪器略去) , 将实验Ⅱ得到的沉淀和含0.20 mol甘氨酸的水溶液混合后加入C中 , 然后利用A中的反应将C中空气排净 , 接着滴入柠檬酸溶液并加热 。反应结束后过滤 , 滤液经蒸发结晶、过滤、洗涤、干燥得到产品
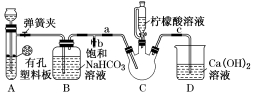
文章插图
回答下列问题:
(1)实验Ⅰ中:实验室配制绿矾溶液时 , 为防止FeSO4被氧化变质 , 应加入的试剂为________(写化学式) 。再滴加少量稀硫酸的作用是________________________________
(2)实验Ⅱ中:生成沉淀的离子方程式为_____________________________________
(3)实验Ⅲ中:
①C中盛柠檬酸溶液的仪器名称为_____________________________
②装置A中所盛放的试剂是________
A.Na2CO3和稀H2SO4 B.CaCO3和稀H2SO4 C.CaCO3和稀盐酸
③确认C中空气排尽的实验现象是_______________________________________
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解 , 另一个作用是________________
⑤洗涤实验Ⅲ中得到的沉淀 , 所选用的最佳洗涤试剂是________
A.热水 B.乙醇溶液 C.柠檬酸溶液
⑥若产品的质量为17.34 g , 则产率为________%
8、三氯氧磷(POCl3)是一种重要的化工原料 , 工业上可以直接氧化PCl3制备POCl3 , 反应原理为:
P4(白磷)+6Cl2===4PCl3,2PCl3+O2===2POCl3 。
PCl3、POCl3的部分性质如下:
物质
熔点/℃
沸点/℃
其他
PCl3
-112
75.5
遇水生成H3PO3和HCl
POCl3
2
105.3
遇水生成H3PO4和HCl
某兴趣小组模拟该工艺设计实验装置如下(某些夹持装置、加热装置已略去):
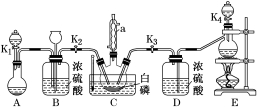
文章插图
(1)仪器a的名称为________________ , B装置中长颈漏斗的作用是________________
(2)装置E用来制取Cl2 , 反应的离子方程式为________________________________
(3)为使实验顺利进行 , 还需补充的装置为_____________
(4)反应时 , 需严格控制三个条件:
①先制取________________ , 缓慢地通入C 中 , 直至C 中的白磷消失后 , 再通入另一种气体
②C装置用水浴加热控制温度为60~65 ℃ , 除加快反应速率外 , 另一目的是_____________________
③反应物必须干燥 , 否则会在C 装置中产生大量的白雾 , 其主要成分为________(写化学式)
(5)反应结束后通过下面步骤测定POCl3产品中Cl 的含量 , 元素Cl 的质量分数为____________(写出计算式)
Ⅰ.取x g产品于锥形瓶中 , 加入足量NaOH溶液 , POCl3完全反应后加稀硝酸至酸性;
Ⅱ.向锥形瓶中加入0.100 0 mol·L-1 的AgNO3 溶液40.00 mL , 使Cl-完全沉淀;
Ⅲ.再向锥形瓶中加入20 mL硝基苯 , 振荡 , 使沉淀表面被有机物覆盖;
Ⅳ.然后加入指示剂 , 用c mol·L-1 NH4SCN溶液滴定过量Ag+至终点 , 记下所用体积为V mL 。
[已知:Ag3PO4溶于酸 , Ksp(AgCl )=3.2×10-10 , Ksp(AgSCN )=2×10-12]
9、肼是重要的化工原料 。某探究小组利用下列反应制取水合肼(N2H4·H2O):
- 染发剂什么牌子好 染发剂排名第一
- 现在什么专业比较吃香 未来什么技术最吃香
- 春天开的常见的花的名字 春天开花的植物有哪些
- 什么叫绩效工资 员工绩效工资分配方案
- 送妈妈生日礼物送什么好 送妈妈礼物排行大全
- 三本和大专有什么区别 500分的大专和200分的大专
- 网络营销的方式包括哪些 简述网络营销的方式有哪些
- 4款实用的微信营销工具软件 微信推广软件有哪些
- 水果店进货渠道有哪些 水果批发商利润有多大
- 自然堂属于什么档次的护肤品 国产十大最有效抗衰老护肤品